蛋白质研究专题
一、抗体基础知识与分类
1.1 抗体的定义、结构
抗体(Antibody),也被称为免疫球蛋白(Immunoglobulin,Ig),是一类由B细胞产生的蛋白质,能够与特定抗原(如细菌、病毒、毒素等)结合,具有高度的特异性。
经典的抗体结构,由2条重链(Heavy Chain)和2条轻链(Light Chain)组成。如图中所示,以IgG分子为例,IgG分子的重链,由1个可变区结构域(Fab区),3个恒定区结构域组成(Fc区)。重链决定了抗体的类别(IgG、IgA、IgM等)。
IgG分子的轻链,由1个可变区结构域,1个恒定区结构域组成,分为κ链和λ链。
重链和轻链都包含两个主要的功能区域,其中Fab区又称抗原结合区,这个区域与抗原结合,具有特异性。Fc区又称效应区,这个区域与免疫系统的其他部分相互作用,启动免疫反应。
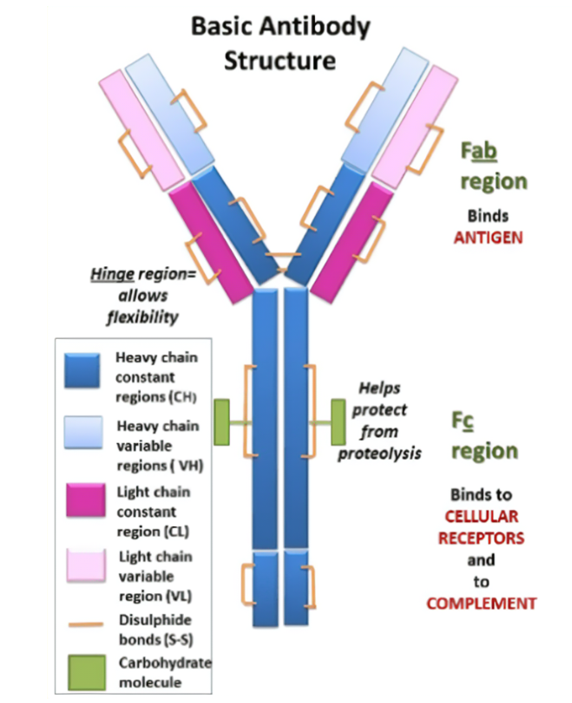
图1:经典抗体结构
根据重链抗原性的差异,抗体可以分为五大类:IgM、IgG、IgA、IgD和IgE。其中:
(1)IgM:是初次体液免疫应答早期的主要抗体,以五聚体形式存在;
(2)IgG:是血清中含量最高的抗体,具有抗菌、抗病毒、抗毒素等多种功能,能够通过胎盘传递给胎儿,提供被动免疫;
(3)IgA:主要存在于黏膜表面和分泌液中,是抵抗微生物和抗原入侵的第一道防线,母乳中的IgA可以保护新生儿的胃肠道免受病原体侵害;
(4)IgD:主要在成熟B细胞表面作为BCR表达,与抗原结合后可诱导B细胞活化;
(5)IgE:是引起Ⅰ型超敏反应的主要变应原,通过与肥大细胞或嗜碱性粒细胞结合,诱发炎症反应。
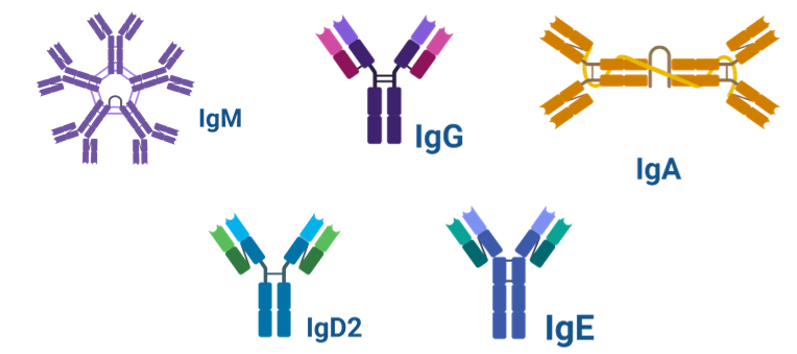
图2:不同抗体分子的结构
1.2 抗体的主要分类及其特点
根据抗体的结构和功能,抗体可以分为单克隆抗体、多克隆抗体和重组抗体几大类:
(1)单克隆抗体/Monoclonal Antibodies, mAbs
由单一B细胞克隆产生的抗体,具有高度的特异性,通常用于治疗、诊断和科研中,具有更高的亲和力和特异性。
1)特点:高度特异性、单一来源、可大规模生产
2)应用:癌症治疗、免疫学研究、诊断试剂
(2)多克隆抗体/Polyclonal Antibodies, pAbs
由多种B细胞同时产生的抗体群体,这些抗体群体针对抗原的不同表位。
1)特点:针对抗原的多个表位、生产周期短、成本较低
2)应用:抗原检测、免疫沉淀、免疫组化等
(3)重组抗体/Recombinant Antibodies
通过基因工程技术产生的抗体,通常由合成基因编码,能够在体外系统中生产。
1)特点:高可操作性、可定制化、无动物源污染
2)应用:疫苗开发、基因治疗、特定抗原识别
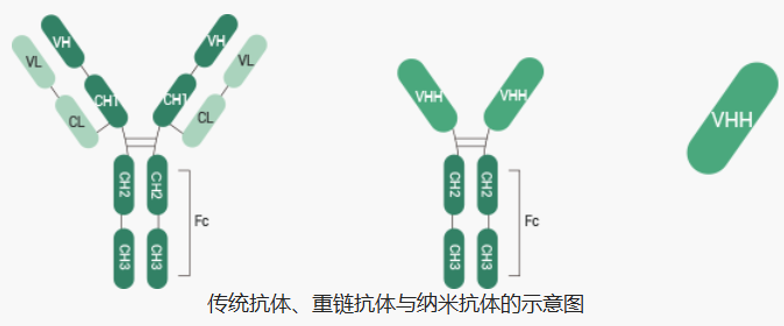
图3:传统抗体、重链抗体与纳米抗体示意图
(4)纳米抗体/Nanobody
除传统抗体外,今年比较火热的就是纳米抗体。纳米抗体不含Fc段,避免了Fc段引起的免疫反应,分子量约为传统抗体的十分之一。
1)特点:特异性强,抗原亲和力高,免疫原性低,高耐热性和稳定性
2)应用:有强大的组织渗透力,肿瘤的诊断与靶向治疗
1.3 抗体的制备方法与技术
抗体的制备是抗体研究和应用的关键环节,目前主要有主要包括多克隆抗体生产,基于杂交瘤的小鼠/兔单抗、噬菌体展示、重组抗体等制备方法。
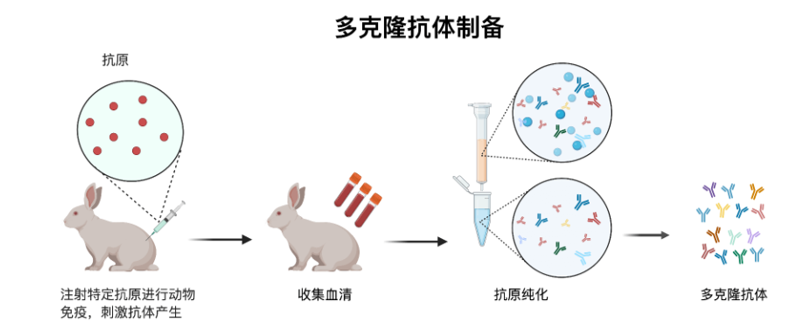
1.3.1 多克隆抗体生产(Polyclonal Antibody Production)
多克隆抗体就是将带有多种表位的抗原,免疫动物,如兔子、小鼠或大鼠,它们在接种特定抗原后,体内产生多种不同的B细胞克隆,每个克隆产生针对抗原不同表位的抗体。因此最终生成的是针对多种表位的抗体的混合物。
多克隆抗体生产比较快速,但是存在批次间一致性差,纯度较低,可能存在免疫原性等缺点。
1.3.2 杂交瘤法小鼠/兔单克隆抗体制备
与多克隆抗体技术在免疫小鼠或兔子后,收集其脾脏B细胞并与骨髓瘤细胞融合,形成杂交瘤细胞,细胞因此获得永生。通过筛选,可以获得分泌特定抗体的单克隆抗体。
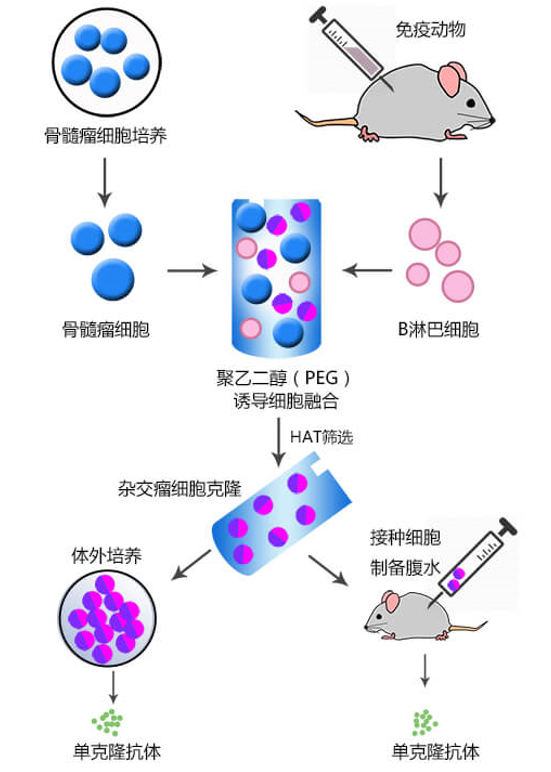
图4:杂交瘤法小鼠/兔单克隆抗体制备
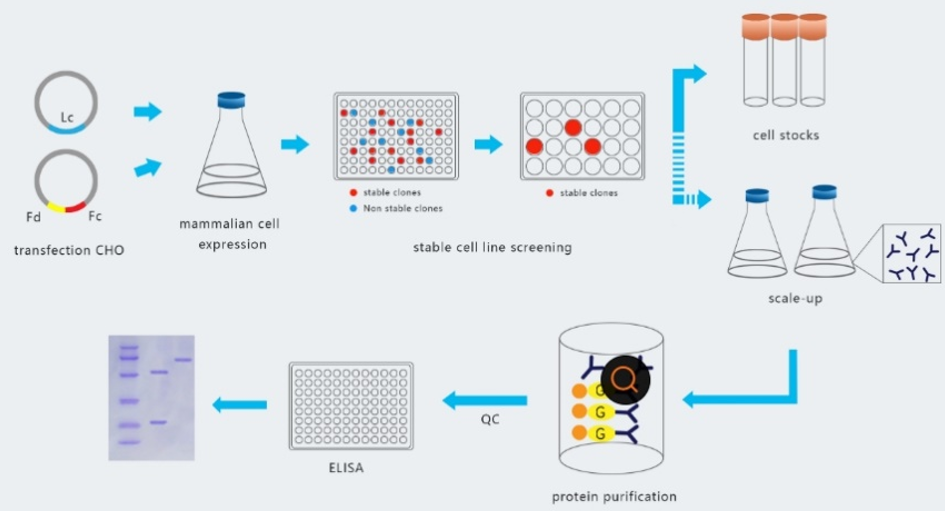
1.3.3 重组抗体生产(Recombinant Antibody Production)
重组抗体生产,就是利用重组DNA技术和合成基因,先构建包含抗体表达基因的质粒/病毒,然后转染细菌/细胞,通过细菌。细胞进行抗体生产的方法。这一过程不需要依赖动物模型,而是通过获取所需抗体的蛋白序列,创建重链和轻链表达质粒,将这些质粒转染入人类细胞,最终纯化抗体。
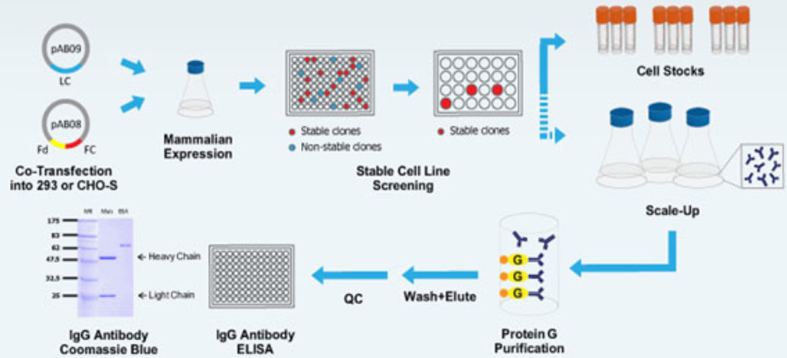
图5:重组抗体的生产流程
重组抗体的表达体系包括,大肠杆菌的原核表达系统,酵母细胞,昆虫细胞,哺乳动物细胞的真核表达系统,植物细胞表达系统,以及近几年出现的无细胞表达系统。
重组抗体的特点和优势:
(1)确定化的高特异性和亲和力:重组抗体设计用于对目标抗原具有高度特异性和亲和力,这使得它们能够精确靶向并减少非目标效应。
(2)批次间一致性和可放大生产:重组抗体的体外生产方法适合大规模生产,意味着这些抗体的供应不太可能成为限制因素。
(3)高度工程化:重组抗体序列可以基于AI和大数据进行调整和优化,提供了许多工程化的机会,包括同种型转换和物种转换,可以扩展多重实验的范围。
(4)不需要使用动物:重组抗体生产的一个重要伦理优势是它避免了使用动物。
1.3.4 噬菌体展示技术(Recombinant Antibody Production)
噬菌体展示技术就是提取免疫动物B细胞,并提取抗体RNA,转录成cDNA,克隆到噬菌体载体中,构建噬菌体抗体库。这个库包含了大量的抗体候选基因,它们被插入到噬菌体的外壳蛋白基因中,展示在噬菌体的表面。然后通过亲和筛选,筛选出能够特异性结合抗原的噬菌体。
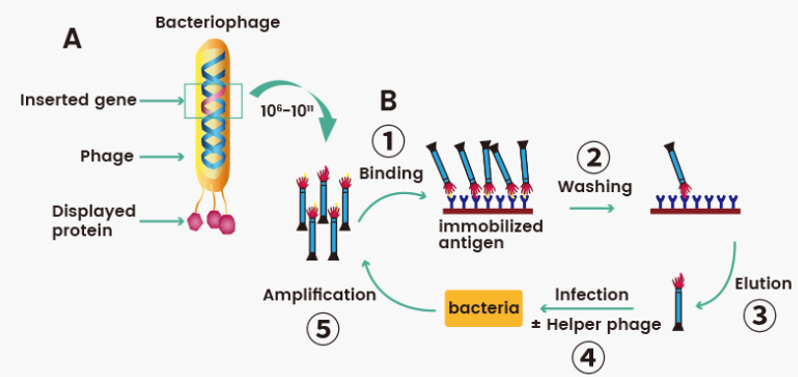
图6:噬菌体展示技术原理
最后筛选出的噬菌体被感染到大肠杆菌中进行扩增,然后从中提取抗体基因进行序列分析和功能验证,以确定其特异性和亲和力。最后进行大规模培养噬菌体或转染宿主细胞,来生产大量的单克隆抗体。
1.3.5 单B细胞排序(Single B Cell Sorting)
单B细胞排序(Single B Cell Sorting)技术是一种用于生产单克隆抗体的先进方法,它利用每个B细胞只产生一种特异性抗体的特性,从免疫动物的淋巴组织中分离单个B细胞,并通过单克隆化技术扩增这些细胞的重链和轻链可变区基因,最终在哺乳动物细胞内表达获得具有生物活性的单克隆抗体。
单B细胞排序(Single B Cell Sorting)技术流程如下:
动物免疫 → PBMC分离 → 流式分选 → 单B细胞培养筛选 → 阳性克隆测序 → 载体构建、抗体表达纯化
由于直接从免疫动物重获取,且不需要经过多轮次的筛选,因此具有如下特点和优势:
(1)高特异性:由于直接从免疫动物体内获取B细胞,保持了抗体的天然特异性。
(2)快速生产:相比传统方法,单B细胞排序技术可以更快地生产单克隆抗体。
(3)高亲和力:通过体内亲和力成熟过程,获得的抗体具有高亲和力。
(4)全天然源性:抗体来源于天然免疫反应,保持了其天然结构和功能。
随着单细胞靳准控制的Beacon仪器,以及微流控技术的发展,单B细胞排序(Single B Cell Sorting)技术用于抗体生产已经在工业领域被很多生产厂家接受,为来有可能加速抗体的发现和生产。
1.4 抗体的应用领域——从科研到体外诊断
单克隆抗体药物已成为癌症、免疫性疾病等治疗的主流手段。例如,抗肿瘤抗体药物如Trastuzumab(Herceptin)靶向HER2受体治疗乳腺癌;抗免疫抑制抗体如Infliximab(Remicade)通过靶向TNF-α治疗类风湿关节炎和克罗恩病等免疫疾病。
但是,抗体不仅用于我们耳熟能详的抗体药物,抗体在医学、科学研究、以及工业领域中都具有多种应用。
1.4.1 抗体与医学诊断
抗体被应用于体外诊断试剂盒中。例如,ELISA技术通过抗原-抗体反应,可以用于病毒感染、肿瘤标志物检测、免疫系统疾病等的诊断。
此外,抗体还被应用于免疫组化、流式细胞术等方法中,用于细胞标记、病理分析等。
1.4.2 抗体与科学研究
在基础研究中,抗体是不可或缺的工具,主要应用于以下几个方面:
(1)抗原识别与定位
通过免疫组化和免疫荧光等技术,抗体可以用于细胞和组织中的抗原识别与定位。例如,利用抗体标记肿瘤组织中的特定标志物,帮助确定肿瘤的类型和分期。
(2)目标蛋白识别
抗体在分子生物学实验中,应用于Western Blot、免疫沉淀(IP)、免疫共沉淀(Co-IP)等技术,帮助识别目标蛋白,并研究其功能和相互作用。
1.4.3 生物技术与工业应用
抗体在生物技术和工业领域的应用逐渐增多,尤其是在蛋白质工程和食品安全方面。
(1)生物制药
抗体被用于生物制药中,例如ADC药物,就是以抗体药物可以作为“载体”药物,将药物或毒素精确输送到目标细胞,达到靶向治疗的效果。重组抗体的生产提高了药物的生产效率。
(2)食品安全
抗体也被用于食品安全检测,通过抗体试剂,可以检测食品中的病原微生物、农药残留物等污染物。
(3)环境监测
在水质监测、土壤污染检测等方面,抗体能够通过与特定污染物结合,检测环境中有害物质的存在和浓度。
二、常见免疫检测技术的基本原理
2.1 免疫检测的基本原理:抗原-抗体特异性结合的力量
免疫检测的基本原理是抗原与抗体的特异性结合。
抗原是能够激活免疫系统的物质,通常是外来分子或病原微生物的表面分子,而抗体则是由免疫系统产生的,用于识别并结合抗原的蛋白质。
抗原与抗体之间的结合是高度特异的,这一特性是免疫检测技术得以被应用的基础。
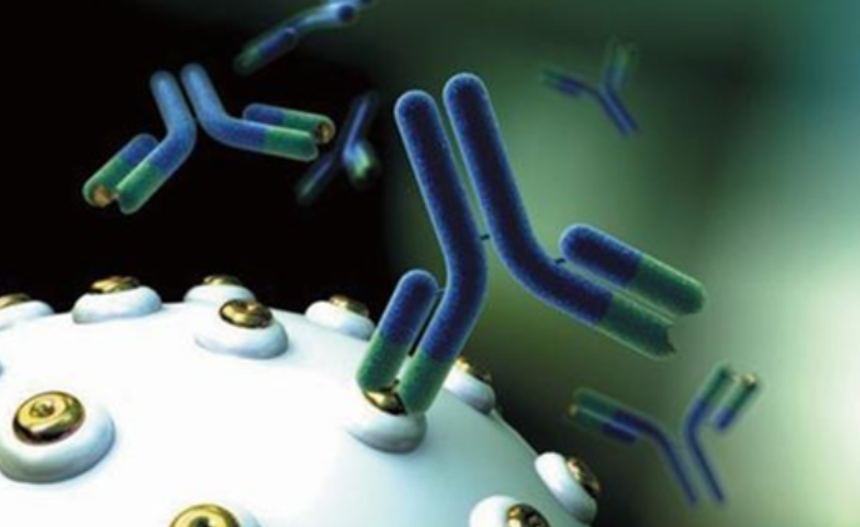
图2:抗体特异性结合到细胞表面的抗原
此外,抗体与抗原的结合需要具备如下特点,才能使抗体成为一种好用的免疫检测试剂:
(1)特异性:每个抗体需要且只能识别并结合与其结合位点匹配的抗原,才能保证检测的准确性。
(2)高亲和力:抗体与抗原结合的亲和力需要较高,才能使达到一定的检测灵敏度。
(3)稳定性:抗体-抗原结合后的复合物相对稳定,才能有足够的时间,对是否结合进行稳定精准的测量。
2.2 信号放大原理:从色素、荧光到电化学信号的转化过程
抗体是一个单分子蛋白,体积很小,绝大多数时候被结合的靶标分子体积也很小,都不能通过肉眼直接看见。因此,对抗体检测到的目标分子进行定量和定性的分析,需要将这种结合信息进行转化和放大,变成一种光信号或者点信号。
信号放大是免疫检测中重要的一步,它通过增加检测信号的强度来提高检测的灵敏度。不同的标记物和探针具有不同的信号放大机制,常见的信号放大方式包括色素反应、荧光信号放大、电化学信号放大等。
(1)色素反应:传统的酶联免疫吸附试验(ELISA)中,酶标记物催化底物反应生成可见色素,颜色的深浅与抗原浓度成正比。通过视觉或光学传感器测量颜色的变化,可以推算样品中抗原的含量。
(2)荧光标记:荧光标记物在特定波长的激发下会发射出荧光。通过测量荧光强度,可以定量分析抗原的浓度。荧光标记常用于免疫荧光(IF)检测和流式细胞术(FACS)。
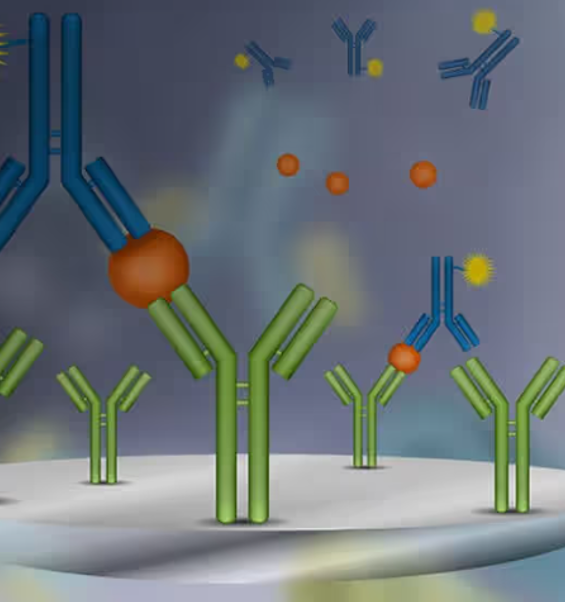
图3:带有荧光标记的抗体结合抗原,从而将看不见得结合转化成荧光信号
(3)电化学信号:电化学信号放大技术常用于化学发光免疫检测,通过催化反应生成光信号,利用光电转换设备将其转换为电信号,进一步放大检测结果。
信号放大的原理在不同类型的免疫检测中有所差异,但其核心目标是通过增加信号的强度来提高检测灵敏度,尤其是在低浓度抗原的情况下。
2.3 常见的检测标记物类型:酶标、荧光标记、化学发光标记和电化学标记
免疫检测中的标记物是用来将抗原-抗体反应转化为可检测信号的关键工具。常见的检测标记物包括酶标、荧光标记、化学发光标记和电化学标记等,每种标记物都有其独特的优缺点和应用场景。
1、酶标记/ Enzyme-conjugated labels
常用的酶标记物包括辣根过氧化物酶(HRP)和碱性磷酸酶(AP),即通过催化底物反应生成可见色素。酶标记一般情况下操作简便、成本低、灵敏度较高,但是反应速率受环境影响较大,需要避免底物过度氧化。
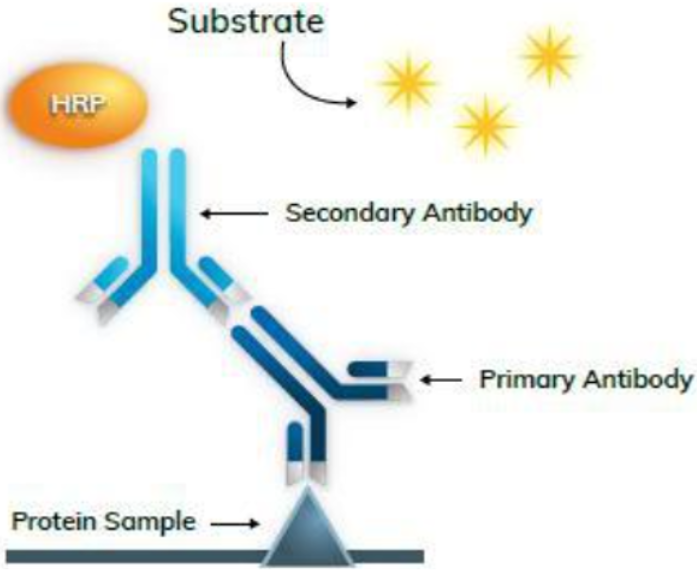
图4:通过酶标记抗体,酶进行催化反应产生颜色反应
2、荧光标记/ Fluorescent labels
荧光标记就是用荧光染料包括FITC、Rhodamine、Cy5等对抗体进行标记。具有灵敏度高、分辨率高、可以实现多重检测的优点,但是受光源干扰较大,并且需要专用设备进行检测。
3、化学发光标记/ Chemiluminescent labels
化学发光标记即化学反应产生光信号,一般情况下灵敏度极高,信号稳定。但是同样需要特定的设备进行检测,成本相对较高。
4、电化学标记/ Electrochemical labels
电化学标记就是检测检测电流或电压的变化,常见于表面等离子共振(SPR)技术。有点事可以快速检测,但是技术复杂,操作难度较高。
2.4 免疫检测的关键性能指标:灵敏度、特异性、准确性、重复性
抗体和检测标记物,以及检测仪器共同组成了免疫检测系统。灵敏度、特异性、准确性、重复性是评估该免疫检测技术的重要性能指标。
1、灵敏度/ Sensitivity
灵敏度是指免疫检测方法能检测到目标抗原的最低浓度的能力,也可以理解为测试能够正确识别出存在目标的“真阳性”样本的能力。灵敏度越高,检测方法能在更低浓度下仍然有效地识别出目标抗原。
2、特异性/ Specificity
特异性是免疫检测方法区分目标抗原与非目标物质(如背景干扰物质或其他类似物质)的能力。高特异性的免疫检测方法能避免因其他相似分子而产生误报,即减少假阳性。
3、准确性/ Accuracy
准确性是免疫检测方法在多次测定中,检测结果与真实值之间的一致性。它不仅涉及到正确识别抗原,还涉及对其浓度的定量准确性。
4、重复性/ Repeatability
重复性是指在相同条件下对同一样本进行多次检测时,检测结果的稳定性和一致性。高重复性的检测方法能够在不同实验和时间段内得到一致的结果。
三、抗体免疫检测技术
3.1 酶联免疫吸附技术 (ELISA):经典的抗体检测方法
酶联免疫吸附试验(ELISA)是一种应用于抗原和抗体检测的经典技术。
(1)ELISA实验原理
ELISA的核心是抗原或抗体在微孔板上的吸附和结合,通过加样、洗涤、抗体反应、酶标二抗的结合以及底物显色,最终通过分光光度计测量颜色变化来分析抗原或抗体的浓度。
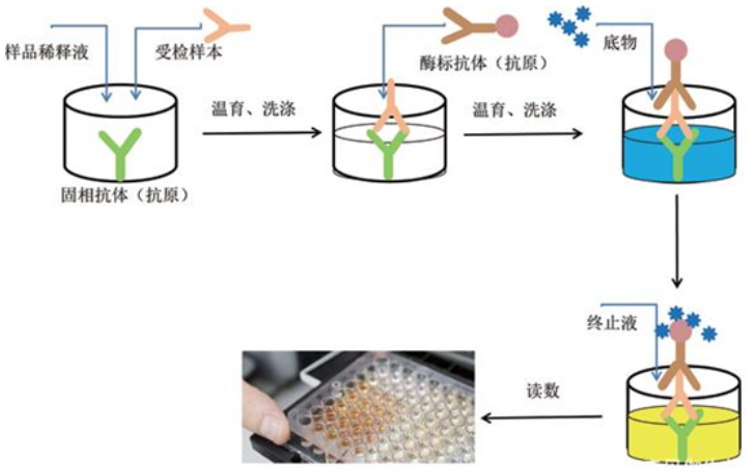
图:间接法ELISA实验基本流程示例
(2)实验流程
一般情况下,ELISA的实验流程如下:
1. 样本加样:
(1)在96孔板中添加抗原(或抗体),然后通过吸附作用使其固定在孔内。
(2)根据实验的需要,选择合适的抗原/抗体浓度。
2. 孵育:
在37°C下孵育一定时间,促进抗原或抗体与孔内的其他组分反应。
3. 洗涤:
使用缓冲液清洗去除未结合的成分,以减少背景噪声。
4. 添加酶标记的二抗:
二抗与待测物(抗原或抗体)结合,标记的酶可以催化底物的反应,产生显色信号。
5. 显色反应:
(1)加入底物,使其与酶发生反应,产生可见的颜色变化。
(2)使用分光光度计测定吸光度。
6. 数据分析:
根据信号的强度与标准曲线对比,从而定量分析抗原或抗体浓度。
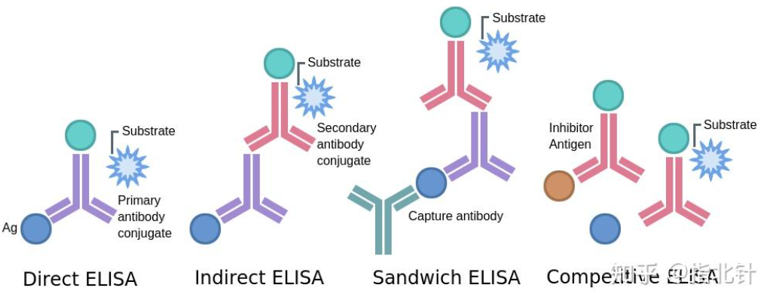
目前ELISA方法已衍生出直接法、间接法、夹心法、竞争法等多种方法。但每个方法都是基于抗原抗体相互结合的免疫原理,因此原理都大同小异。不同方法的差异性在于,通过引入二抗等因素放大信号可以增加检测的灵敏度或者通过多个抗体或者竞争可以减少假阳性。
3.2 Western Blot (WB):检测蛋白质表达的“金标准”
Western Blot(WB)是一种用于蛋白质分子量分析和表达水平检测的技术。它能准确地确认目标蛋白的大小,并可以进一步分析其表达量。
(1)实验原理
Western Blot技术通过SDS-PAGE凝胶电泳将不同大小的蛋白质分离,然后将其转移到PVDF膜上,使用抗体识别目标蛋白,通过标记的二抗与酶的底物反应,最终获得蛋白质的表达信息。
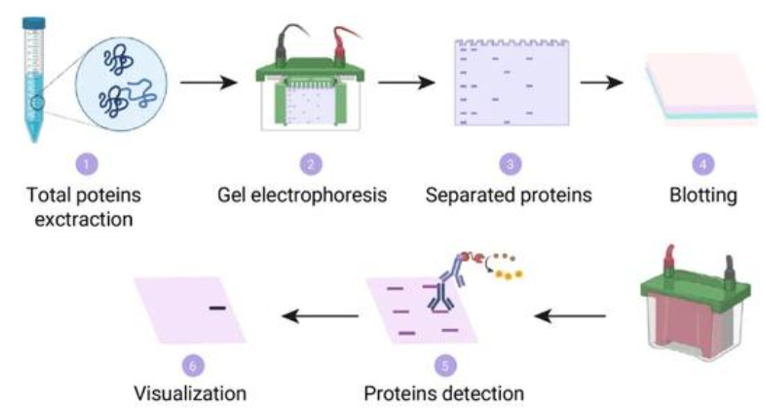
图:Western Blot实验基本流程示例
(2)实验流程
1. 蛋白提取:
用RIPA裂解液,从细胞或组织中提取总蛋白。
2. SDS-PAGE凝胶电泳:
使用SDS-PAGE凝胶在电场存在情况下,根据蛋白分子量将不同蛋白进行进行分离。
3. 转膜:
通过电转移的方式将分离的蛋白质从PAGE凝胶转移到PVDF膜上,常用的转膜方法是湿转膜。
4. 封闭膜:
用5%奶粉或BSA封闭膜上的非特异性结合位点,避免抗体与膜的无关位点结合。
5. 一抗孵育:
加入针对目标蛋白的特异性一抗,孵育约1小时,确保抗体与目标蛋白结合。
6. 二抗孵育:
加入带有酶标的二抗,二抗与一抗结合,形成抗原-抗体复合物。
7. 显色反应:
通过化学发光或底物显色反应,酶催化底物生成光信号,通过X光胶片或化学发光成像仪记录结果。
3.3 免疫荧光 (IF):活细胞内的动态抗体检测
免疫荧光(IF)是一种能够在细胞和组织切片中实时检测抗体的技术。通过使用荧光标记抗体,可以观察细胞内部的抗原分布与定位。
(1)实验原理
免疫荧光技术利用荧光标记的抗体与目标抗原特异性结合,使用荧光显微镜观察信号。荧光标记的抗体能够在细胞内或组织切片中准确定位抗原。
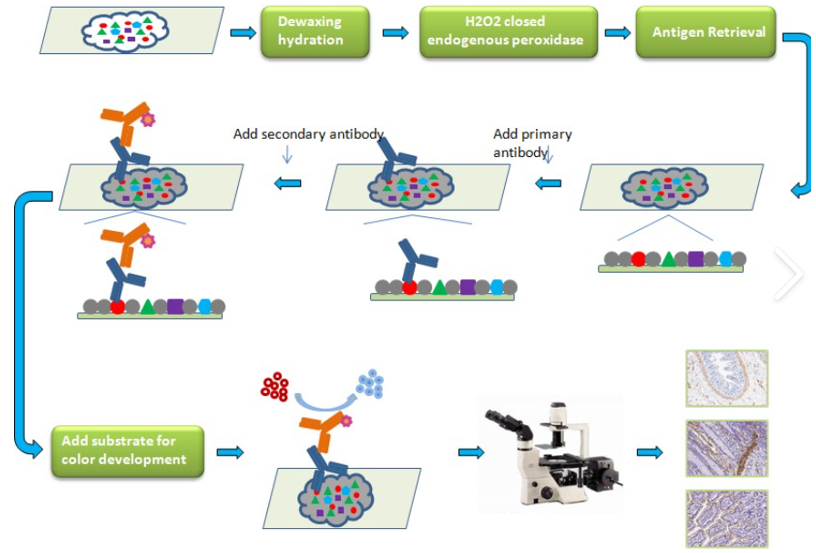
图:免疫荧光实验流程图,展示从样本固定到荧光显微镜观察的步骤
(2)实验流程
1. 细胞准备:
(1)对于单层生长细胞,将细胞接种到预先放置有处理过的盖玻片的培养皿中,待细胞接近长成单层后取出盖玻片,用PBS洗两次。
(2)对于悬浮生长细胞,取对数生长细胞,用PBS离心洗涤两次,用细胞离心甩片机制备细胞片或直接制备细胞涂片。
2. 固定:
根据需要选择适当的固定剂固定细胞。常用的固定剂有4%中性甲醛固定液(TBS缓冲液配制),固定15分钟后,用PBS洗涤3次,每次5分钟。
3. 通透:
使用交联剂(如多聚甲醛)固定后的细胞,一般需要在加入抗体孵育前,对细胞进行通透处理,以保证抗体能够到达抗原部位。常用的通透剂有100%甲醇,处理5-15分钟。
4. 封闭:
使用封闭液对细胞进行封闭,时间一般为30分钟。常用的封闭液有5%山羊血清。
5. 一抗结合:
室温孵育1小时或者4℃过夜。之后用PBST漂洗3次,每次冲洗5分钟。
6. 二抗结合:
间接免疫荧光需要使用二抗。室温避光孵育1小时。之后用PBST漂洗3次,每次冲洗5分钟,再用蒸馏水漂洗一次。
7. 封片及检测:
滴加封片剂一滴,封片,荧光显微镜检查。
8. 复染核:
滴加DAPI避光孵育5分钟,对标本进行染核,生理盐水洗去多余的DAPI。
9. 荧光显微镜观察:
在荧光显微镜下观察并采集图像。
3.4 流式细胞术 (Flow Cytometry, FACS):高通量单细胞抗体检测技术
流式细胞术是一种可以快速分析单个细胞表面或细胞内标志物的技术,能够同时检测多个参数,应用于免疫学、细胞生物学等领域。
(1)实验原理
流式细胞术利用荧光标记的抗体与细胞表面或细胞内的抗原结合,通过激光照射和荧光探测器获取细胞的多维数据。
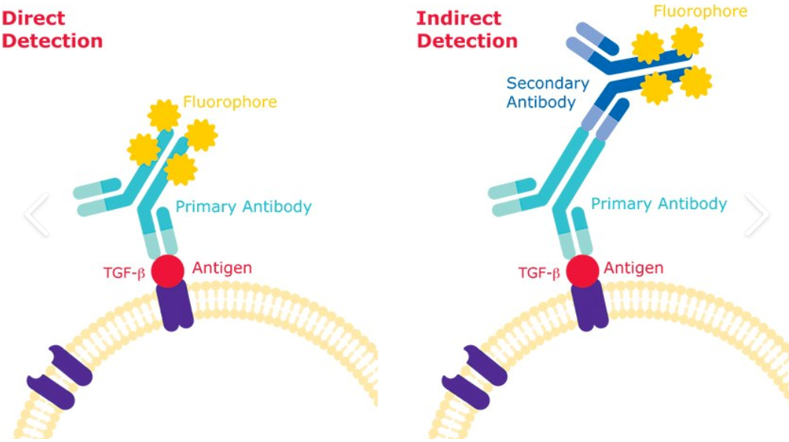
图:直接法和间接法流式抗体结合原理
(2)实验流程
1. 细胞准备:
从组织或细胞培养中分离单个细胞。
2. 抗体染色:
使用荧光标记的抗体染色细胞,通过抗体与抗原的结合进行标记。
3. 流式检测:
将染色细胞通过流式细胞仪,通过激光进行多参数检测。
4. 数据分析:
将数据输入计算机,通过软件进行分析,生成细胞群体的表型图谱。
3.5 免疫沉淀和共免疫沉淀 (IP/Co-IP):研究蛋白互作的利器
免疫沉淀技术通过利用抗体与目标蛋白结合,将其从复杂的生物样本中分离出来。共免疫沉淀则是在此基础上,利用目标蛋白与其他结合蛋白之间的相互作用,进一步捕获蛋白质复合物。这种技术常常用于探索蛋白质复合体的组成、研究细胞内信号传导路径,以及了解不同蛋白之间的相互作用。
实验流程
1. 样本制备:
提取细胞或组织中的总蛋白,通常使用裂解缓冲液(如RIPA缓冲液)来溶解细胞膜并释放细胞内容物。
2. 抗体结合:
将抗体加入样本中,抗体与目标蛋白结合。对于共免疫沉淀,除了目标蛋白的抗体,还可以加入针对可能与目标蛋白结合的其他蛋白的抗体。
3. 添加磁珠或Agarose珠:
抗体通常会与磁珠或琼脂糖珠结合,从而帮助沉淀抗原-抗体复合物。珠子经过孵育后,可以通过磁场或离心力将复合物沉淀出来。
4. 洗涤:
通过多次洗涤去除未结合的非特异性物质,确保最终沉淀中的蛋白质是与抗体特异性结合的目标蛋白。
5. 分析:
沉淀后的蛋白质可以通过Western Blot或质谱等技术进行进一步分析,以识别目标蛋白或探测其相互作用的蛋白。
3.6 免疫组化(Immunohistochemistry,IHC):组织切片中定位和定量特定蛋白质的技术
免疫组化的原理是利用抗原与抗体之间的特异性结合,通过将抗体与显色剂(如酶或荧光素)结合,来检测和定位组织切片中的特定蛋白质。这一技术允许研究人员在细胞或组织层面上观察和分析蛋白质的表达和分布。
实验流程
(1)组织切片制备:将组织样本固定、包埋、切片,制作成适合染色的组织切片。
(2)脱蜡和水化:将组织切片从石蜡中脱出,并逐步水化以便于抗体渗透。
(3)抗原修复:通过热处理或酶消化等方法暴露切片中的抗原决定簇。
(4)封闭:使用封闭液(如正常血清)封闭非特异性结合位点,减少背景噪音。
(5)一抗孵育:将特异性的一抗(针对目标蛋白的抗体)加入切片中,孵育使抗体与抗原结合。
(6)洗涤:用缓冲液洗涤切片,去除未结合的一抗。
(7)二抗孵育:加入与一抗相匹配的二抗,二抗上连接有显色剂。
(8)显色:使用底物溶液使显色剂催化反应,产生可见的颜色变化。
(9)复染:使用苏Mu精-伊红(H&E)等染料对细胞核进行染色,以便更好地观察细胞形态。
(10)脱水和封片:去除多余的水分,用封片剂覆盖切片,并用盖玻片封片。
(11)显微镜观察:使用显微镜观察切片,记录目标蛋白的表达和定位情况。
3.7 免疫检测技术常见问题汇总
在进行抗体免疫检测技术的实验时,常常会遇到一些挑战和问题。小编列举了常见的问题和解决方案,希望能为遇见问题的小伙伴提供帮助。
常见问题及解决方案
1. 背景信号过强:
(1)原因:背景信号可能来源于非特异性结合、抗体浓度过高或封闭不完全。
(2)解决方案:优化抗体的浓度、增加封闭步骤,并且使用不同的封闭液以减少背景信号。此外,确保样本中没有非特异性结合物质。
2. 低灵敏度:
(1)原因:信号较弱通常由于抗体与目标蛋白结合的效率低、底物反应不充分或酶活性不高。
(2)解决方案:使用更有效的酶标抗体,提高抗体浓度,或使用更敏感的底物反应。对于ELISA等技术,增加孵育时间和温度也有助于提高灵敏度。
3. 非特异性结合:
(1)原因:抗体可能与其他非目标分子发生交叉反应,导致假阳性结果。
(2)解决方案:使用高质量的抗体,并在优化的洗涤条件下进行实验。此外,可以通过选择更为专一的抗体进行实验。
4. 样本蛋白降解:
(1)原因:蛋白质在提取和操作过程中可能会被降解,导致数据不准确。
(2)解决方案:使用蛋白酶抑制剂、优化裂解条件、以及保持低温环境,尽量减少蛋白降解。
5. 荧光信号衰减(对于免疫荧光实验):
(1)原因:荧光标记的抗体可能因曝光过长而导致信号衰减。
(2)解决方案:尽量减少样本暴露于光源的时间,使用抗光漂白剂来增加荧光信号的稳定性。
四、新兴免疫检测技术
4.1 数字化ELISA (Simoa技术):高灵敏度单分子免疫检测技术
数字化ELISA(简称Simoa,Single Molecule Array)技术是将传统的酶联免疫吸附试验(ELISA)与数字化相结合的新技术,实现了高灵敏度的抗体检测,能够检测到单分子的信号。
Simoa技术通过微流控芯片中的微孔来分离和捕获每一个抗体或抗原分子,在这些微孔中,抗体或抗原分子被捕获后,酶标记反应会在每个微孔内发生。这些反应所产生的信号通过高灵敏度的检测仪器被捕捉和分析。
由于每个微孔中只有一个抗原或抗体分子参与反应,Simoa技术能够精确地测量到低浓度的目标分子,甚至可以检测到每个微孔中存在的单个分子。其原理在于每个微孔体积是50fL左右,因此可以检测到一个分子的信号(fg/ml)。而常规的ELISA反应体积是100ul,因此需要数百万个分子才可以被检测到(pg/ml)。
因此Simoa的优势在于,单个分子的荧光信号可以被识别,进一步增加了检测的灵敏度。

图:Simoa实验流程
实验流程
(1)利用带有捕获抗体的磁珠捕获样品中的抗原,再用生物素标记检测抗体对被捕获的抗原进行标记;加入链霉亲和素—半乳糖苷酶复合物,与检测抗体上的biotin结合
(2)将磁珠加入微孔芯片,因为芯片直径很小,一个孔只能落入一个磁珠,通过油封去除多余的磁珠
(3)加入半乳糖苷酶的催化底物产生荧光信号,并进行读板
Simoa应用领域
(1)临床:用于早期癌症筛查、心血管疾病、神经退行性疾病(如阿尔茨海默症)的生物标志物检测;
(2)食品领域:用于检测食品和水中的微量污染物;
(3)IVD领域:用于肿瘤、免疫疾病的早期诊断。
4.2 Luminex磁珠多重检测 (xMAP技术):高通量多指标检测技术
Luminex磁珠多重检测技术(xMAP技术)是一种基于磁性微珠的多重免疫检测系统。通过不同颜色的磁珠与特定的抗原或抗体结合,从而实现多种目标分子的并行检测。
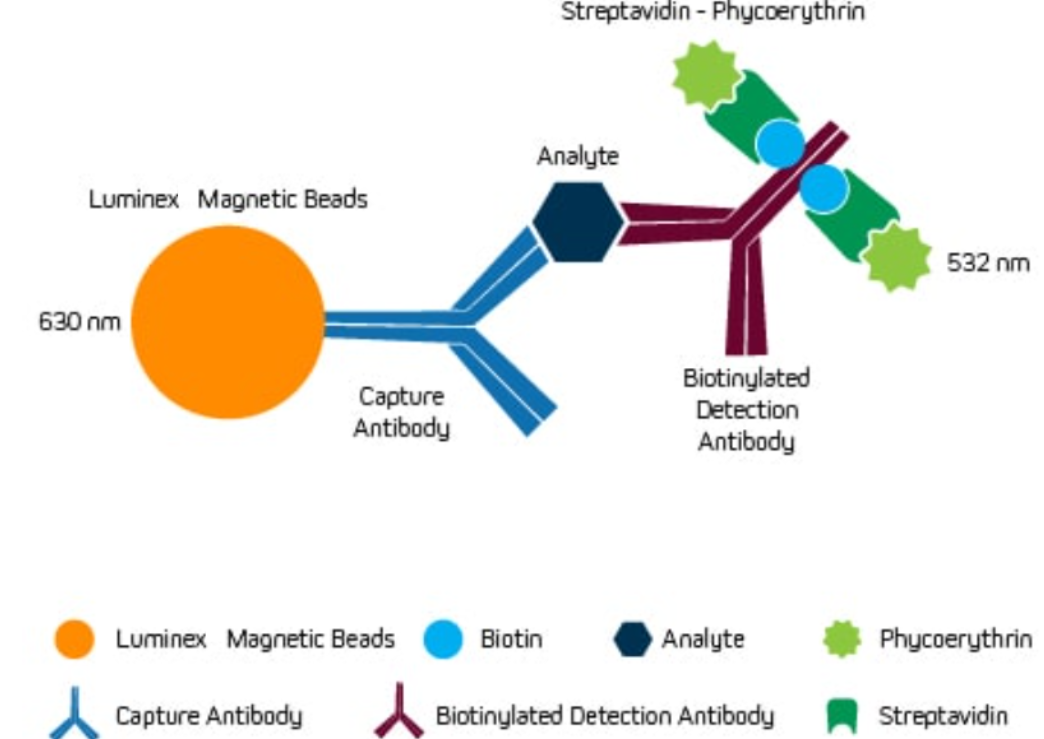
图:典型的Luminex(xMAP)分析设置
xMAP技术的应用领域
(1)免疫学研究:xMAP技术能够同时检测多种细胞因子、抗体和抗原,应用于免疫学领域的研究;
(2)临床检测:在癌症、生物标志物筛查、感染性疾病等领域,xMAP技术被用于疾病诊断和监测。
4.3 蛋白质微阵列 (Protein Microarray):大规模的蛋白质/抗体高通量筛选技术
蛋白质微阵列技术是一种高通量的检测技术,可以同时分析成千上万种蛋白质或抗体的相互作用。通过将捕获的蛋白质固定在固体基底上,蛋白质微阵列能够进行抗体、抗原和蛋白质的筛选与分析。
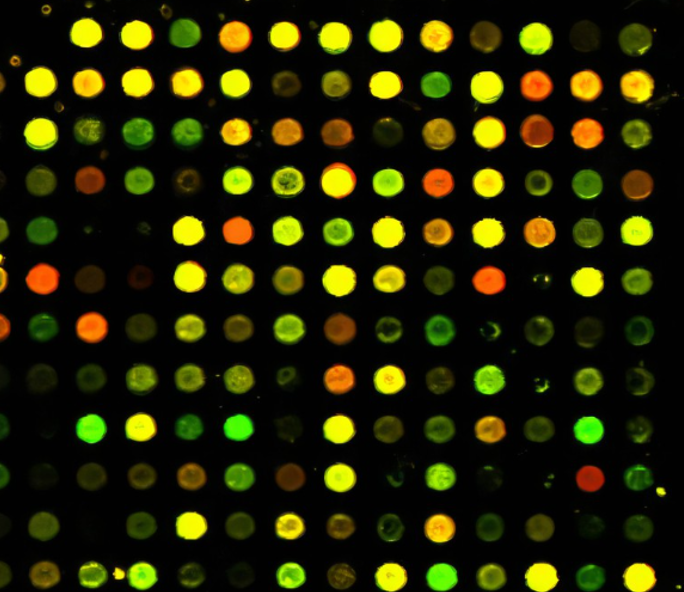
图:蛋白微阵列芯片结果图
应用领域
(1)高通量筛选:蛋白质微阵列应用于药物筛选、免疫学研究以及蛋白质-蛋白质相互作用的研究;
(2)临床研究:在癌症、免疫性疾病、感染性疾病等领域,蛋白质微阵列用于快速筛选潜在的生物标志物;
(3)个体化医疗:蛋白质微阵列技术能够帮助个体化治疗的开发,提供精准的疾病监测手段。
4.4 单细胞蛋白检测 (Single-Cell Proteomics)——从群体到单细胞的转变
单细胞蛋白质检测技术即在单个细胞水平上进行蛋白质的定量和定性分析,目前有多个平台科进行单细胞蛋白质检测,主要通过高通量质谱或微流控芯片等技术,从单个细胞中提取蛋白质,并进行定量分析以实现。
应用领域
(1)肿瘤研究:在肿瘤细胞的异质性研究中,单细胞蛋白质组学能够揭示不同癌细胞的表型和功能差异,为癌症的个体化治疗提供依据;
(2)神经科学:通过单细胞蛋白质组学技术,研究人员能够更好地理解神经系统的复杂性,揭示神经退行性疾病的病理机制;
(3)免疫学:在免疫细胞的研究中,单细胞蛋白质组学能够帮助揭示免疫细胞的异质性,推动精准免疫治疗的发展。
比较常见的单细胞蛋白质检测技术有:IsoSPARK技术,10X Proteomics,Scope2等。
4.5 双分子荧光互补 (BiFC) 和荧光共振能量转移 (FRET)——细胞内实时检测蛋白相互作用
BiFC和FRET技术是研究细胞内蛋白质相互作用的重要工具。通过这些技术,研究人员能够在活细胞中实时监测到蛋白质之间的结合和相互作用。
技术原理
(1)BiFC:通过将荧光蛋白的两部分分别与目标蛋白质的不同部分融合,当目标蛋白质相互作用时,两部分荧光蛋白会重新结合,形成一个完整的荧光蛋白,从而产生可见的荧光信号。
(2)FRET:基于荧光共振能量转移原理,当两种不同的荧光分子非常接近时,激发光会从一个荧光分子转移到另一个分子,产生新的荧光信号。FRET技术可以用于检测蛋白质之间的近距离相互作用。
应用领域
(1)细胞内蛋白相互作用研究:BiFC和FRET技术能够实时检测蛋白质在活细胞内的相互作用过程,为细胞生物学研究提供了强大的工具。
(2)药物筛选:通过检测蛋白质-蛋白质相互作用,BiFC和FRET技术可以在药物研发过程中用于筛选潜在的药物分子,特别是在抗癌药物的开发中具有重要价值。
当前新的免疫检测技术层出不穷,例如基于CRISPR的抗体检测(SHERLOCK/Cas12/Cas13)、基于表面等离子共振 (SPR)的分子互作实时检测、替代传统ELISA的AlphaLISA,DELFIA TRF,HTRF/Lance技术等。
具体使用过程中,可以基于项目需求,从检测目标、通量、灵敏度何特异性等多角度进行检测技术筛选。
五、免疫检测试剂罗列和挑选
5.1 免疫检测实验中常用试剂罗列
1、一抗(Primary Antibodies)
简单来说,一抗就像个“侦探”,专门去识别和绑定你想要检测的目标分子(抗原)。它们有“火眼金睛”,只盯着特定的抗原不放。一抗的作用在于,找到目标抗原并牢牢绑定,是整个免疫检测的核心环节。没有它,后面的显色啥的都没戏。
2、二抗(Secondary Antibodies)
二抗很多时候,就像一抗的“助攻”,它不直接抓抗原,而是识别一抗,再附带一个“放大器”(比如酶或荧光染料)。因为二抗可以同时绑定多个一抗,因此将酶或者荧光染料放在二抗上,能将最后检测到的信号,进行有效放大。因此,二抗在免疫检测中的作用在于增强信号,提升灵敏度。常见的类型有酶标二抗(HRP、AP)、荧光标记二抗(FITC、PE)、金标二抗等。
3、酶(Enzymes)和底物(Substrates)与显色试剂
免疫检测中,通常将酶和抗体进行偶联。抗体进行特异性结合,而酶催化底物显色或发光,让你能直观地看到实验结果,产生信号。比较常用的酶有HRP(辣根过氧化物酶)和AP(碱性磷酸酶)。
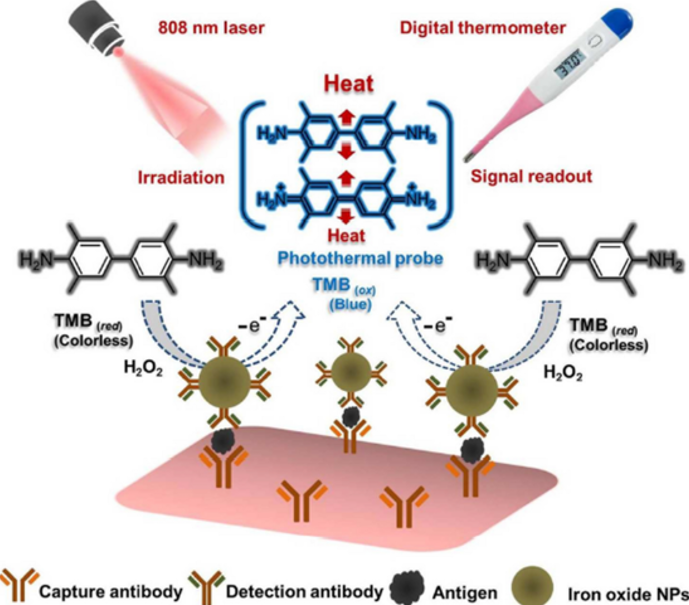
TMB显色原理
其中HRP(辣根过氧化物酶)和TMB(3,3',5,5'-四甲基联ben胺)等底物搭配,能产生蓝色或黄色反应,特别灵敏,常用于ELISA、WB。
HRP(辣根过氧化物酶)和DAB(3,3'-二氨基联ben胺)反应后产生棕色沉淀,常用于免疫组化(IHC)。
AP(碱性磷酸酶)和BCIP/NBT底物反应显蓝紫色,适合背景噪声要求高的实验。适合免疫印迹(WB)。
4、荧光素(Fluorophores)
除了通过酶催化产生显色反应外,还可以给抗体加上荧光素,通过给抗体打上“荧光标签”,可以方便在荧光显微镜下直接观测到有那些抗体与代价测抗原进行了结合。
常见荧光素:FITC(绿色荧光)、PE(橙红色荧光)、Cy5(远红外荧光)等。
检测抗体偶联荧光素
5、偶联试剂(Conjugation Reagents)
如此前免疫检测原理中所介绍,抗体能够结合抗原,但是免疫检测中使用的抗体需要与酶或者荧光试剂进行偶联结合,才能将不可见的信号,变成可检测的信号。
常见偶联剂有SMCC(交联抗体和酶的“化学小帮手”)、EDC/NHS(把抗体和小分子底物“粘”在一起)。
5.2 免疫检测抗体的生产和挑选
在免疫检测试剂中,抗体是核心试剂。根据不同的生产工艺,免疫检测的抗体可以分成单克隆抗体,多克隆抗体和重组抗体不同类型。
在此之前我们先补习一下抗体的基因重排,从而帮助我们更好地理解单克隆抗体、多克隆抗体和重组抗体的差异性。
1、抗体基因的免疫重排原理
在免疫反应中,抗体的多样性来源于免疫系统中的B细胞通过一种叫做“免疫重排”的过程来生成不同的抗体。每个抗体由两部分组成:重链和轻链,这些链条是由基因编码的。为了产生能够识别不同抗原的抗体,B细胞的基因会通过一种称为“V(D)J重排”的机制进行重新组合。
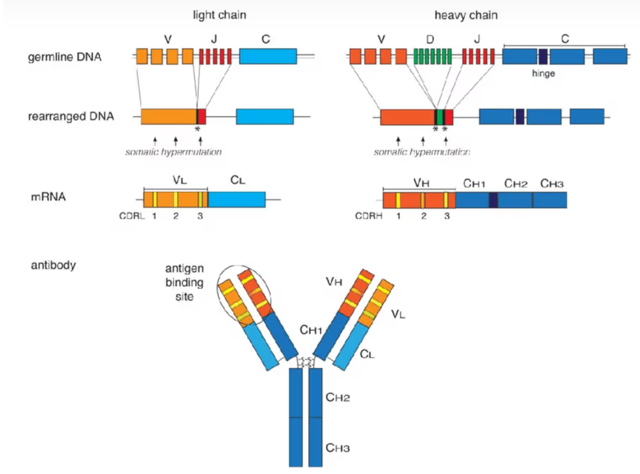
抗体VDJ基因的重排
在这个过程中,位于重链和轻链基因中的不同“基因片段”(V片段、D片段和J片段)被随机选择并组合,形成一个完整的抗体基因。这种基因重排是随机的,能够产生较大的抗体库,使得每个B细胞产生的抗体具有独特的结合特性,可以识别不同的抗原表位。
当B细胞接触到外来抗原时,它们会被激活并增殖,产生较多相同抗体分子(克隆)。这些抗体能够特异性地结合抗原,从而发挥免疫作用。值得注意的是,免疫重排的随机性使得每个B细胞的抗体特异性是特殊的,这也是为什么我们的免疫系统可以应对各种不同的病原体。
而很多时候,天然的抗原具有不同的表位,因此一个抗原进入体内后,会产生很多种不同的抗体,也就是通常所说的多克隆抗体。
2、免疫检测抗体的不同类型
(1)单克隆抗体(mAb):抗原免疫机体后,取中一个B淋巴细胞,和骨髓瘤细胞融合。得到永生化的单个B细胞后,生产得到的抗体是单克隆抗体。由于来源于一个细胞,所以单克隆抗体的特异性超强,适合准确检测。
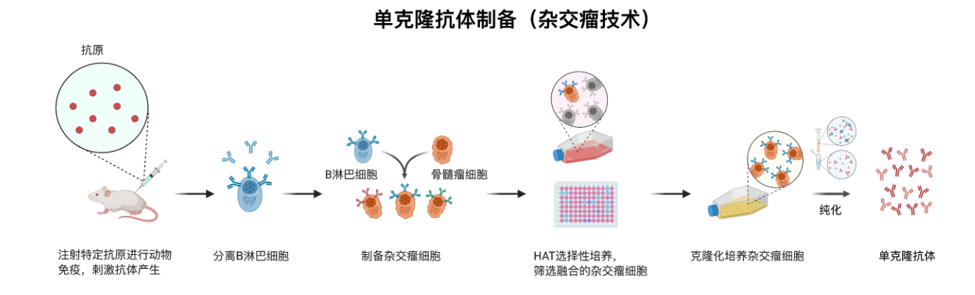
(2)多克隆抗体(pAb):抗原免疫机体后,收集上清,得到的来自多个B细胞生产的抗体。因此能识别抗原的不同表位,灵敏度更高。
(3)重组抗体:通过基因工程技术合成抗体序列编码基因,并转染到抗体表达细胞系中生产的抗体称之为重组抗体。重组抗体的特异性和一致性都在线,适合高端检测或药物开发。
5.3 不同免疫检测技术的抗体选择指南
(1)ELISA:ELISA实验中,一般情况下建议用特异性高的单克隆抗体做捕获抗体,用信号更强的多抗作为检测抗体,两者组合起来效果更好;
(2)Western Blot:为了可以识别变性蛋白的多个表位,一般情况下建议使用多抗,可以使信号更明显;
(3)流式细胞术:流式技术中,一般使用的荧光标记抗体都是单克隆抗体;
(4)免疫组化(IHC):IHC实验选择抗体时要考虑组织固定和抗原修复后的特异性,一般都建议选择生产厂家验证过的IHC专用抗体;
(5)免疫沉淀(IP/Co-IP):选择高亲和力的抗体,确保能有效拉下目标蛋白及其相互作用伙伴。




























































































